Главная
Каталог лекарств
Медикаменти
Ліки та профілактичні засоби
Протипухлинні засоби
КАБОМЕТИКС
Кабометикс 60 мг №30 таблетки
Кабометикс 60 мг №30 таблетки
Дата оновлення препарату: 10.03.2024

Нет в наличии
Характеристики
Категория
Дозировка
60 мг
Производитель
Patheon France
Страна-производитель
Франция
Торговое название
Форма выпуска
Таблетки
Срок годности
3 года
Активные вещества
Кабозантиниб
Количество в упаковке
30
Способ введенния
перорально
Код Морион
485798
Код АТС/ATX
L01X E26
Кому можно
ВОДИТЕЛЯМ
с осторожностью
Беременным
запрещено
КОРМЯЩИМ МАТЕРЯМ
запрещено
Обратите внимание!
Инструкция, размещенная на этой странице, носит информационный характер и предназначена исключительно для ознакомления. Не используйте эту инструкцию в качестве медицинских рекомендаций. Постановка диагноза и выбор методики лечения осуществляются только вашим семейным врачом. Медмаркет LikiE не несет ответственности за возможные негативные последствия, возникшие в результате использования информации, размещенной на сайте www.likie.ua.
Детальнее об Отказе от ответственности.
Инструкция для Кабометикс 60 мг №30 таблетки
Важно! Эта инструкция по применению является официальной инструкцией производителя, утверждена и предоставлена Государственным реестром лекарственных средств Украины. Эта инструкция представлена исключительно с ознакомительной целью и не является основанием для самолечения.
По 7 таблеток, покрытых пленочной оболочкой в блистере; по 4 блистера в картонной коробке или по 30 таблеток, покрытых плёночной оболочкой в бутылке из полиэтилена высокой плотности (HDPE) с полипропиленовым средством, недоступным для открывания детьми, с тремя контейнерами с силикагелем-осушителем по 1 г и полиэфирным; по 1 бутылке в картонной коробке.
Таблетки, покрытые пленочной оболочкой.
Основные физико-химические свойства: овальные таблетки, покрытые плёночной оболочкой, желтого цвета, с тиснением «XL» на одной стороне и «60» на другой стороне таблетки.
Механизм действия
Кабозантиниб – низкомолекулярный ингибитор тирозинкиназы, ингибирующий множественные рецепторные тирозинкиназы (RTKs), участвующие в процессах роста опухолей и ангиогенеза, патологического изменения костной ткани, устойчивости к лекарственным средствам и метастатической прогрессии опухоли. В результате оценки ингибирующей активности против различных киназ кабозантиниб был определен ингибитором рецепторов МЭТ (рецептор фактора роста гепатоцитов) и рецепторов VEGF (фактор роста эндотелия сосудов). Кроме того, кабозантиниб ингибирует другие тирозинкиназы, включая GAS6-рецептор (AXL), RET, ROS1, TYRO3, MER, рецептор фактора стволовых клеток (КИТ), TRKB, Fms-подобную тирозинкиназу-3 (FLT3) и ТИЭ-2. >
Фармакодинамические эффекты
Кабозантиниб показал угнетение роста опухоли, связанную с дозой, регресс опухоли и/или подавленное метастазирование в широком диапазоне доклинических моделей опухоли.
Кардиологическая электрофизиология
Увеличение от исходного уровня в коррегированном интервале QT с корректировкой Фридериция (QTcF) на 10–15 мсек на 29-й день (но не на 1-й день) после начала лечения кабозантинибом (в дозе 140 мг в день) наблюдалось у контролируемом клиническом исследовании с участием больных медуллярным раком щитовидной железы. Этот эффект не был связан с морфологическими изменениями предсердной волны или возникновением новых сердечных ритмов. В этом исследовании ни один пациент, получавший кабозантиниб, не имел подтвержденного QTcF > 500 мсек, что не подтверждено при лечении НКК или ГЦК (в дозе 60 мг).
Клиническая эффективность и безопасность
Клинические данные по почечноклеточной карциноме (НКК) после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF)
Безопасность и эффективность лекарственного средства КАБОМЕТИКС при лечении почечно-клеточной карциномы после предварительного лечения средствами, влияющими на VEGF, оценивали в рандомизированном открытом многоцентровом исследовании ІІІ фазы (METEOR). Пациенты с распространенной светоклеточной почечноклеточной карциномой (НКК), ранее получавшие по меньшей мере 1 курс лечения ингибиторами рецепторов тирозинкиназы VEGF (VEGFR TKI), были рандомизированы (1:1) для приема КАБОМЕТИКСА (N = 330). Пациенты могли получать другие предыдущие курсы терапии, включая цитокины или антитела, направленные на VEGF, на рецепторы запрограммированной клеточной смерти-1 (PD-1) или его лиганды. Допускались ранее леченные пациенты с метастазами в мозг. Выживаемость без прогрессирования заболевания оценивалась комитетом по проведению слепой независимой радиологической экспертизы, а первичный анализ был проведен среди первых 375 рандомизированных пациентов. Вторичными конечными точками были доля пациентов с объективным ответом и общая выживаемость (ОВ). Оценки опухоли проводились каждые 8 недель в течение первых 12 месяцев, затем – – через каждые 12 недель.
Базовые демографические показатели и характеристики заболевания были сходными в группах, принимавших КАБОМЕТИКС и эверолимус. Большинство пациентов были мужского пола (75%), средний возраст – 62 года. 71% пациентов получили только один предварительный курс VEGFR TKI; 41% пациентов получили суннитин как единственный предварительный курс VEGFR TKI. Согласно критериям прогностической категории риска Мемориального онкологического центра Слоана Кеттеринга (MSKCC), 46% имели благоприятное течение (0 факторов риска), 42% - промежуточный (1 фактор риска), 13% –; плохой (2 или 3 фактора риска). 54% пациентов имели 3 или более органов с метастазами, включая легкие (63%), лимфатические узлы (62%), печень (29%) и кости (22%). Средняя продолжительность лечения составляла 7,6 месяца (диапазон 0,3–20,5) у пациентов, получавших КАБОМЕТИКС, и 4,4 месяца (диапазон 0,21–18,9) у пациентов, получавших эверолимус.
Статистически значимое улучшение выживаемости без прогрессирования заболевания наблюдается при применении КАБОМЕТИКСА по сравнению с эверолимусом (рисунок 1 и таблица 1). Планируемый промежуточный анализ общей выживаемости проводился при анализе выживаемости без прогрессирования заболевания и не достиг предела статистической значимости (202 явления, НR = 0,68 [0,51, 0,90], р = 0,006). В следующем незапланированном промежуточном анализе общей выживаемости было показано статистически значимое улучшение у больных, принимавших КАБОМЕТИКС, по сравнению с группой эверолимуса (320 явлений, медиана 21,4 месяца и 16,5 месяца, НR = 0,66 [0,53, 0, 83], р=0,0003, рисунок 2). Сравненные результаты по ЗВ наблюдались при дальнейшем (дескриптивном) анализе 430 явлений.
Исследовательский анализ выживаемости без прогрессирования заболевания и общей выживаемости в группе «все рандомизированные пациенты, получившие не менее одной дозы исследуемого лекарственного средства» также показал надежные результаты в пользу КАБОМЕТ ИКСУ по сравнению с эверолимусом в разных подгруппах в соответствии с возрастом (до < 65 лет по сравнению с > 65 лет, пол, группа риска Мемориального онкологического центра Слоана&Кэттеринга (благоприятный, промежуточный, плохой), ECOG статус (0 или 1) , время от постановки диагноза до рандомизации (до <1 года по сравнению с >1 года), МЕТ статус опухоли (высокий по сравнению с низким или неизвестным), метастазы в костях (отсутствие по сравнению с наличием), висцеральные метастазы (отсутствие в сравнении с присутствием), метастазы в костях и висцеральные метастазы (отсутствие по сравнению с наличием), количество предыдущих курсов VEGFR-TKI (1 сравнительно >2), длительность первого VEGF (< 6 месяцев сравнительно > 6 месяцев). доли пациентов с объективным ответом приведены в таблице 2.
Рисунок 1. Кривая выживаемости без прогрессирования заболевания, определенной независимым комитетом радиологической экспертизы у пациентов с НКК после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF) (первые 375 рандомизированных пациентов) (метод Каплана-Мейера) , исследование METEOR)
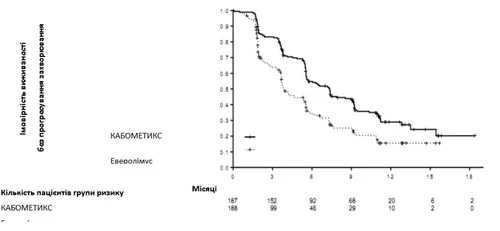
Таблица 1
Резюме результатов выживаемости без прогрессирования заболевания (ВБПЗ), определенное независимым комитетом радиологической экспертизы у пациентов с НКК после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF) (исследование METEOR)
Первоначальный анализ ОПН популяции
Популяция ИТТ
Конечная точка
КАБОМЕТИКС
Эверолимус
КАБОМЕТИКС
Эверолимус
N = 187
N = 188
N = 330
N = 328
Медиана времени ОБПЗ (95% ДИ – доверительный интервал), месяцы
7,4 (5,6; 9,1)
3,8 (3,7; 5,4)
7,4 (6,6; 9,1)
3,9 (3,7; 5,1)
Соотношение рисков (HR) (95% ДИ), p-значение 1
0,58 (0,45; 0,74), p>0,0001
0,51 (0,41; 0,62), p<0,0001
1 Стратифицированный логарифмический ранговый критерий
Рисунок 2. Кривая общей выживаемости пациентов с НКК после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF) (метод Каплана – Мейера, исследование METEOR)
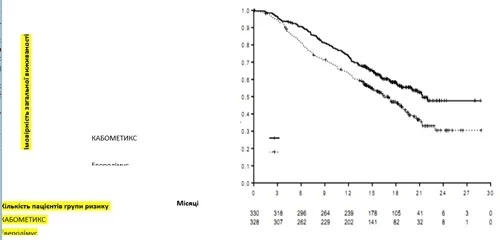
Таблица 2
Резюме данных о количестве пациентов с объективным ответом согласно отчету независимого комитета радиологической экспертизы (IRC) и отчета исследователей среди больных НКК после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF)
Конечная точка
Первоначальный анализ показателя объективного ответа в популяции ИВС, данные IRC
Показатель объективного ответа в популяции ИВС, данные исследователей
КАБОМЕТИКС
Эверолимус
КАБОМЕТИКС
Эверолимус
N = 330
N = 328
N = 330
N = 328
Показатель объективного ответа (лишь частичный объективный ответ) (ДИ 95%)
17% (13%, 22%)
3% (2%, 6%)
24% (19%, 29%)
4% (2%, 7%)
- значение 1
p<0,0001
p< 0,0001
Частный ответ
17%
3%
24%
4%
Медиана времени до первого ответа, месяцы (ДИ 95%)
1,91 (1,6; 11,0)
2,14(1,9; 9,2)
1,91 (1,3; 9,8)
3,50 (1,8;5,6)
Стабилизация заболевания как лучший ответ
65%
62%
63%
63%
Прогрессирование заболевания как лучший ответ
12%
27%
9%
27%
1 Критерий хи-квадрат
Клинические данные по лечению пациентов с почечноклеточной карциномой, ранее не получавших лечение
Безопасность и эффективность применения лекарственного средства КАБОМЕТИКС у пациентов с почечноклеточной карциномой, ранее не получавших лечение, оценивали в рандомизированном открытом многоцентровом исследовании (CABOSUN). Пациенты (N=157) с ранее нелеченной, местно-распространенной или метастатической светоклеточной НКК были рандомизированы (1:1) для получения лекарственного средства КАБОМЕТИКС (N=79) или суннитиниба (N=78). Пациенты должны были иметь заболевание среднего или высокого риска в соответствии с определениями категорий риска по классификации Международного консорциума баз данных метастатических форм НКК (IMDC). Пациенты были стратифицированы по группе риска IMDC и наличию костных метастазов (да/нет). Около 75% пациентов перенесли операцию по удалению почки до начала лечения.
Пациент должен был иметь один или два из указанных факторов риска в случае среднего риска и три или более факторов в случае высокого риска: время с момента диагностики НКК до системного лечения < 1 года, гемоглобин < НМН (нижняя граница нормы), корректируемый уровень кальция > ВМН (верхний предел нормы), индекс KPS < 80%, нейтрофилы > ВМН, тромбоциты > ВМН.
Первоначальной конечной точкой была выживаемость без прогрессирования заболевания. Вторичные конечные точки эффективности были определены как показатель объективного ответа и общая выживаемость. Оценка опухоли проводилась каждые 12 недель.
Исходные демографические показатели и характеристики заболевания были аналогичными в группах применения лекарственного средства КАБОМЕТИКС и суннитиниба. Большинство пациентов были мужчинами (78%); средний возраст – 62 года. Распределение пациентов по группам риска IMDC было следующим: 81% пациентов в группе среднего риска (1-2 фактора риска), а 19% –; в группе высокого риска (3 факторов риска). Большинство пациентов (87%) имели оценку по функциональному статусу ECOG 0 или 1; 13% – оценку 2. Костные метастазы выявлены у 36% пациентов.
Статистически значимое улучшение выживаемости без прогрессирования заболевания, ретроспективно оценивавшего независимый комитет по проведению слепой радиологической экспертизы (IRC), продемонстрировало преимущества в пользу лекарственного средства КАБОМЕТИКС по сравнению с суннитином (рисунок 3, таблица 3). Результаты анализа, проведенного исследователем и IRC относительно определения выживаемости без прогрессирования заболевания согласовывались между собой.
Пациенты с положительным и отрицательным статусом МЭТ демонстрировали благоприятный эффект лекарственного средства КАБОМЕТИКС по сравнению с суннитином; причем большая активность наблюдалась у пациентов с положительным статусом МЭТ по сравнению с пациентами с отрицательным статусом MET (HR = 0,32 (0,16, 0,63) по сравнению с 0,67 (0,37, 1,23)), соответственно .
Терапию лекарственным средством КАБОМЕТИКС связывали с тенденцией к более длительной выживаемости по сравнению с суннитином (таблица 3). Это исследование было недостаточно мощным для анализа общей выживаемости, а полученные данные были незрелыми.
Данные по показателю объективного ответа приведены в таблице 3.
Рисунок 3. Кривая выживаемости без прогрессирования заболевания у пациентов с НКК, ранее не получавших лечение (данные IRC, метод Каплана-Мейера)

Таблица 3
Результаты эффективности у пациентов с НКК, ранее не получавших лечение (популяция ITT, исследования CABOSUN)
Показатель
КАБОМЕТИКС
(N=79)
Сунитиниб
(N=78)
Выживаемость без прогрессирования заболевания по данным IRC а
Медиана выживаемости без прогрессирования (95% ДИ)
8,6 (6,2; 14,0)
5,3 (3,0; 8,2)
HR (95% ДИ); стратифицирован б, в
0,48 (0,32; 0,73)
Двухстороннее, логарифмическое ранговое p-значение: стратифицирован б
p=0,0005
Выживаемость без прогрессирования заболевания по данным исследователя
Медиана выживаемости без прогрессирования (95% ДИ)
8,3 (6,5; 12,4)
5,4 (3,4; 8,2)
HR (95% ДИ), стратифицировано б, в
0,56 (0,37; 0,83)
Двухстороннее, логарифмическое ранговое p-значение: стратифицирован б
p=0,0042
Общая выживаемость
Медиана общей выживаемости в месяцах (95% ДИ)
30,3 (14,6; NE)
21,0 (16,3; 27,0)
HR (95% ДИ), стратифицировано б, в
0,74 (0,47; 1,14)
Показатель объективного ответа, n (%) по данным IRC
Полные ответы
0
0
Частные ответы
16 (20)
7 (9)
Объективный ответ (только частичные ответы)
16 (20)
7 (9)
Стабилизация заболевания
43 (54)
30 (38)
Прогрессирование заболевания
14 (18)
23 (29)
Показатель объективного ответа, n(%) по данным исследователя
Полные ответы
1 (1)
0
Частные ответы
25 (32)
9 (12)
Объективный ответ (только частичные ответы)
26 (33)
9 (12)
Стабилизация заболевания
34 (43)
29 (37)
Прогрессирование заболевания
14 (18)
19 (24)
а В соответствии с принятым в ЕС цензурирование данных.
б Факторы стратификации в соответствии с IxRS включали категории рисков IMDC (средний риск, высокий риск и наличие метастазов в костях (да/нет)).
в Рассчитано на основе модели пропорциональных рисков Кокса с корректировкой на факторы стратификации в соответствии с IxRS. Отношение рисков < 1 указывает на выживаемость без прогрессирования в пользу кабозантиниба.
Клинические данные при гепатоцеллюлярной карциноме (ГЦК)
Безопасность и эффективность лекарственного средства Кабометикс оценивали в рандомизированном двойном слепом плацебо-контролируемом исследовании фазы III (CELESTIAL). Пациенты (N=707) с ГЦК, не реагирующей на радикальное лечение, ранее получавшие сорафениб в связи с распространенной формой заболевания, были рандомизированы (2:1) для получения лекарственного средства КАБОМЕТИКС (N=470) или плацебо ( N=237). Пациенты могли получать еще одну предварительную системную терапию в связи с распространенной формой заболевания в дополнение к сорафенибу. Рандомизация была стратифицирована по этиологии заболевания (вирус гепатита В [с или без вируса гепатита С], вирус гепатита С [без вируса гепатита В] или другая категория пациентов), географическому региону (Азия, другие регионы) и при наличии экстрагепатического распространения заболевания и/ или макроваскулярных инвазий (да/нет).
Первоначальная конечная точка эффективности была определена как общая выживаемость. Вторичными конечными точками эффективности были выживаемость без прогрессирования заболевания и показатель объективного ответа, оцениваемых исследователем с использованием Критериев оценки ответа на лечение при солидных опухолях (RECIST) 1.1. Опухоли оценивали каждые 8 недель. Субъекты продолжали лечение слепым методом после радиологического подтверждения прогрессирования заболевания, пока они испытывали клинические преимущества или пока не возникнет потребность в дальнейшей системной терапии или местной, направленной на противоопухолевую печеню. Переход с плацебо в кабозантиниб не разрешался во время слепой фазы лечения.
Базовые демографические показатели и характеристики заболевания были сходными между группами применения лекарственного средства КАБОМЕТИКС и плацебо и представлены ниже для всех 707 рандомизированных пациентов:
Мужчины: 82%
Средний возраст: 64 года.
Европеоидная раса: 56%, азиаты: 34%
Оценка функционального статуса по критериям ECOG на уровне 0:53% или на уровне 1:47%
Печечная недостаточность степени А по классификации Чайлда – По: 99%, степени В: 1%
Этиология ГКК включала 38% пациентов с вирусом гепатита В (ВГВ), 21% с вирусом гепатита С (ВГС), 40% других (ни ВГВ, ни ВГС).
Наличие макроскопической сосудистой инвазии и/или внепеченочной опухоли: 78%.
Уровни альфа-фетопротеина (AFP) ≥400 мкг/л: 41%.
Местно-регионарная трансартериальная эмболизация или процедуры хемоинфузии: 44%
Лучевая терапия перед лечением кабозантинибом: 37%
Медиана продолжительности лечения сорафенибом: 5,32 месяца
72% пациентов получали один, а 28% - 2 предварительные схемы системной терапии для лечения распространенной формы заболевания.
Статистически значимое улучшение общей выживаемости было продемонстрировано для лекарственного средства КАБОМЕТИКС в отношении плацебо (таблица 4, рисунок 4).
Данные о выживаемости без прогрессирования заболевания и показатель объективного ответа представлены в таблице 4.
Таблица 4
Результаты эффективности у пациентов с ГЦК (популяция ITT, исследование CELESTIAL)
Показатель
КАБОМЕТИКС
(N=470)
Плацебо
(N=237)
Общая выживаемость
Медиана общей выживаемости (95% ДИ), месяцы
10,2 (9,1; 12,0)
8,0 (6,8; 9,4)
HR (95% ДИ)1,2
0,76 (0,63; 0,92)
p-значение 1
p=0,0049
-
Выживаемость без прогрессирования заболевания 3
Медиана выживаемости без прогрессирования (95% ДИ)
5,2 (4,0; 5,5)
1.9 (1.9; 1.9)
HR (95% ДИ)1
0,44 (0,36; 0,52)
p-значение 1
p<0,0001
Расчет доли пациентов без определенных событий через 3 месяца после лечения (метод Каплана-Мейера)
% (95% ДИ)
67,0% (62,2%; 71,3%)
33,3% (27,1%; 39,7%)
Показатель объективного ответа, n(%)3
Полные ответы (CR)
0
0
Частные ответы (PR)
18(4)
1 (0,4)
Объективный ответ (CR+PR)
18(4)
1 (0,4)
p-значение 1,4
p=0,0086
Стабилизация заболевания
282 (60)
78 (33)
Прогрессирование заболевания
98 (21)
131 (55)
1 2-сторонний, стратифицированный, логарифмический ранговой критерий, в котором факторами стратификации являются этиология заболевания (вирус гепатита В [с или без вируса гепатита С], вирус гепатита С [без вируса гепатита В] или иная категория пациентов), географический регион (Азия, другие регионы) и наличие экстрагепатического распространения заболевания и/или макроваскулярных инвазий (да/нет) (по данным IVRS).
2 Рассчитано на основе модели пропорциональных рисков Кокса.
3 По оценке исследователя в соответствии с критериями RECIST 1.1.
4 Стратифицированный критерий Кохрана-Мантеля-Гензеля (CMH).
Рисунок 4. Кривая общей выживаемости (метод Каплана-Мейера, исследование CELESTIAL)
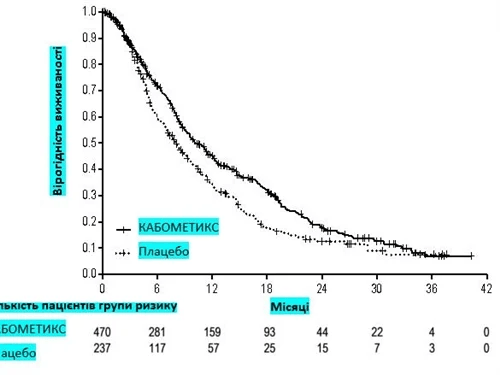
Рисунок 5. Кривая выживаемости без прогрессирования заболевания (метод Каплана-Мейера, исследование CELESTIAL)

Доля системной нелучевой и локальной направленной на печень системной противоопухолевой терапии не по протоколу (NPACT) составила 26% в группе применения кабозантиниба и 33% в группе плацебо. Пациентам, получавшим такие виды терапии, пришлось прекратить лечение изучаемым режимом. Поисковый анализ общей выживаемости с цензурированием данных по применению NPACT обеспечил данные в поддержку результатов первичного анализа: показатель HR, скорректированный на факторы стратификации (на IxRS), составил 0,66 (95% ДИ: 0,52, 0,84; стратифицированное логарифмическое ранговое) p-значение =0,0005). Расчет средней продолжительности общей выживаемости методом Каплана-Мейера составил 11,1 месяца в группе кабозантиниба по сравнению с 6,9 месяцами в группе плацебо, дающей расчеты в отличие в медианах на уровне 4,2 месяца.
Качество жизни оценивали без привязки к конкретному заболеванию (QoL) с помощью опросника EuroQoL EQ-5D-5L. Негативное влияние лекарственного средства КАБОМЕТИКС по сравнению с плацебо на показатель индекса полезности EQ-5D наблюдалось в течение первых недель лечения. После этого периода доступны только ограниченные данные QoL.
Педиатрическая популяция
Европейское агентство по лекарственным средствам отменило обязательство представить результаты исследований лекарственного средства КАБОМЕТИКС во всех подгруппах педиатрической популяции по лечению гепатоцеллюлярной карциномы, а также карцином почек и почечной лоханки, за исключением нефробластомы, нефробластома улярной карциномы и рабдоидной опухоли почек) (см. раздел «Способ применения и дозы» относительно информации о применении лекарственного средства у детей).
Абсорбция
После перорального введения пиковая концентрация кабозантиниба в плазме крови достигается через 3–4 часа. Профили концентрации в плазме в зависимости от времени показывают второй пик абсорбции примерно через 24 часа после введения, что свидетельствует о том, что кабозантиниб может пройти кишечно-печеночную рециркуляцию.
Повторное ежедневное применение кабозантиниба в дозе 140 мг в течение 19 дней привело к увеличению среднего накопления кабозантиниба примерно в 4–5 раз (на основе площади под фармакокинетической кривой «концентрация–время») по сравнению с однократным введением дозы; стабильное состояние достигнуто примерно на 15 день.
Пища с высоким содержанием жира умеренно повысила максимальную концентрацию действующего вещества в плазме крови и значение площади под фармакокинетической кривой «концентрация-время» (41% и 57% соответственно) по сравнению с состояниями натощак у здоровых добровольцев, принимавших перорально одну дозу кабозантиниба, что составляла 140 мг. Информация о влиянии пищи, принятой через 1 час после введения кабозантиниба, отсутствует.
Биологическая эквивалентность не могла быть продемонстрирована между кабозантинибом в капсулах и таблетках после введения разовой дозы 140 мг здоровым добровольцам. Наблюдалось увеличение на 19% максимальной концентрации действующего вещества в плазме крови после введения таблетки (КАБОМЕТИКС) по сравнению с капсулой (КОМЕТРИК). Менее 10% разница показателей площади под фармакокинетической кривой «концентрация-время» наблюдалась после приема таблеток кабозантиниба (КАБОМЕТИКС) и капсул (КОМЕТРИК).
Распределение
Кабозантиниб обладает высокой степенью связывания с белком плазмы человека (≥99,7%). На основании измерения фармакокинетических показателей объем распределения (Vz) составляет примерно 212 л. Связывание с белками плазмы крови не изменялось у пациентов с легкими или умеренными нарушениями функции почек или печени.
Биотрансформация
Кабозантиниб метаболизируется in vivo. Четыре метаболита были в плазме крови при уровнях воздействия (площадь под фармакокинетической кривой «концентрация-время») более 10% от исходных метаболитов: XL184-N-оксид, продукт расщепления амида XL184, моногидроксисульфат XL184 и сульфат продукта расщепления. Два неконъюгированных метаболита (XL184-N-оксид и продукт расщепления амида XL184) имеют <1% целевой активности ингибирования киназы исходного кабозантиниба, каждый из них составляет <10% общего влияния на плазму крови, связанного с лекарственным средством.
Кабозантиниб представляет собой субстрат для метаболизма CYP3A4 in vitro, поскольку нейтрализующее антитело к CYP3A4 ингибирует образование метаболита XL184-N-оксида на >80% в микросомальной инкубации печени человека, катализируемой NADPH; для сравнения, нейтрализующие антитела к CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C19, CYP2D6 и CYP2E1 не влияли на образование метаболитов кабозантиниба. Нейтрализующее антитело к CYP2C9 показало минимальное влияние на образование метаболита кабозантиниба (т.е. снижение <20%).
Вывод
При пероральном применении кабозантиниба в дозах от 20 до 140 мг среднее время полувыведения из плазмы крови кабозантиниба по данным исследований с участием 1883 пациентов и 140 здоровых добровольцев составляет около 110 часов. Средний плазменный клиренс (воображаемый клиренс) равен почти 2,48 л/ч после стабильной экспозиции. Около 81% меченной изотопами дозы выявляли в течение 48 суток после применения однократной дозы 14 C-кабозантиниба у здоровых добровольцев, при этом почти 54% дозы выводилось с калом, а около 27% - выводилось с мочой.
Фармакокинетика в особых группах пациентов
Почечная недостаточность
площади под фармакокинетической кривой «концентрация – время» от 0 до бесконечности от 79,61% до 140,11% у пациентов с умеренной степенью почечной недостаточности по сравнению с пациентами с нормальной функцией почек. Пациенты с ОПН не изучались.
Печеночная недостаточность
По результатам интегрированного анализа популяционной фармакокинетики кабозантиниба у здоровых добровольцев и больных раком (в т.ч. ГЦК) клинически значимого различия среднего уровня экспозиции кабозантиниба в плазме не наблюдали среди пациентов с нормальной функцией печени (n=1425) и легкой формой. n=558). Данные относительно пациентов со средней формой печеночной недостаточности (n=15) по критериям NCI-ODWG (Рабочей группы по дисфункциям органов при Национальном институте рака (США)) ограничены. Фармакокинетика кабозантиниба не оценивалась у пациентов с печеночной недостаточностью тяжелой степени.
Раса
Популяционный фармакокинетический анализ не выявил клинически значимых разногласий в фармакокинетике кабозантиниба в зависимости от расы пациента.
Антинеопластические лекарственные средства. Ингибиторы протеинкиназы. Кабозантиниб.
Код АТХ L01XE26.
Влияние других лекарственных средств на кабозантиниб
Ингибиторы и индукторы CYP3A4
Предварительный прием кетоконазола, мощного ингибитора CYP3A4, в дозе 400 мг 1 раз в сутки в течение 27 дней перед применением разовой дозы кабозантиниба, увеличивал содержание кабозантиниба в плазме крови на 38% (AUC) и уменьшал клиренс кабозантиниба на 2. Мощные ингибиторы CYP3A4 следует применять с осторожностью (включая ритонавир, итраконазол, эритромицин, кларитромицин, грейпфрутовый сок).
Предварительный прием рифампицина, мощного индуктора CYP3A4, в дозе 600 мг 1 раз в сутки в течение 31 дней перед применением разовой дозы кабозантиниба, уменьшал содержание кабозантиниба в плазме крови на 77% (AUC) и увеличивал клиренс кабозантиниба в 4. Следует избегать постоянного одновременного введения мощных индукторов CYP3A4 (включая рифампицин, карбамазепин, фенитоин, фенобарбитал или лекарственные средства, содержащие зверобой ( Hypericum perforatum )).
Регуляторы рН желудочно-кишечного тракта
Предварительный прием эзомепразола, ингибитора протонной помпы (ИПП), в дозе 40 мг 1 раз в сутки в течение 6 дней перед применением разовой дозы 100 мг кабозантиниба указывает на то, что это не оказывает клинически значимого влияния на содержание кабозантиниба в плазме крови (AUC). здоровых добровольцев. При одновременном введении кабозантиниба с агентами, изменяющими рН желудка, корректировка дозы не рекомендуется (включая ИПП, антагонисты рецепторов Н2 и антациды).
Ингибиторы MRP2
Данные исследований in vitro показывают, что кабозантиниб является субстратом MRP2. Поэтому введение ингибиторов MRP2 может привести к увеличению концентрации кабозантиниба в плазме.
Секвестранты желчных кислот
Секвестранты, такие как холестирамин и холестагель, могут вступать в реакцию с кабозантинибом и влиять на поглощение (или реабсорбцию), снижая неблагоприятную дозу (см. раздел «Фармакодинамика»). Клиническое значение этих потенциальных влияний неизвестно.
Воздействие кабозантиниба на другие лекарственные средства
Влияние кабозантиниба на фармакокинетику противозачаточных стероидов не исследовалось. Поскольку контрацептивный эффект не может быть гарантирован, рекомендуется использовать дополнительный метод контрацепции, в частности, барьерный.
Из-за высоких уровней связывания кабозантиниба с белками плазмы крови (см. раздел Фармакокинетика) возможно взаимодействие с варфарином – замещение протеинов плазмы. В этом случае следует контролировать показатели международного коэффициента нормализации (INR).
Ингибиторы P-гликопротеина
Кабозантиниб является ингибитором (IC 50 = 7,0 mМ), но не является субстратом P-гликопротеиновой (P-gp) транспортной активности в двунаправленной системе с использованием клеток, сконструированных для экспрессии Р-гликопротеина (MDCK-MDR1). Одновременное применение ингибиторов P-gp может повышать концентрацию кабозантиниба в плазме крови. Пациентов следует предупреждать о приеме лекарственных средств, которые вливают на Р-gp (таких как фексофенадин, алискирен, амбрисентан, дабигатрана этексилат, дигоксин, колхицин, маравирок, внеконазол, ранолазин, саксаглиптин, ситаглиптин, талинолол, тол.
действующее вещество: кабозантиниб (S)-малат
1 таблетка, покрытая плёночной оболочкой, содержит кабозантинибу (S)-малата, что эквивалентно кабозантинибу 20 мг, или 40 мг, или 60 мг;
другие составляющие: целлюлоза микрокристаллическая, лактоза безводная, гидроксипропилцеллюлоза, натрия кроскармелоза, кремния диоксид коллоидный (безводный), магния стеарат;
пленочная оболочка: опадрай желтый (03K92254): гипромелоза (HPMC) 2910 (Е 464), титана диоксид (Е 171), триацетин, железа оксид желтый (Е 172).
Кабозантиниб оказывает незначительное влияние на способность управлять транспортными средствами или другими механизмами. Во время лечения кабозантинибом некоторые пациенты сообщали о побочных реакциях, таких как утомляемость и слабость. Во время лечения следует соблюдать осторожность при управлении автотранспортом или другими механизмами.
Беременность
Данных по применению кабозантиниба беременными женщинами нет. В ходе исследований на животных была обнаружена репродуктивная токсичность. Потенциальный риск для человека неизвестен. Кабозантиниб не следует применять в течение беременности, кроме случаев срочной клинической необходимости.
Кормление грудью
Неизвестно, попадает ли кабозантиниб или его метаболиты в грудное молоко человека. Нельзя исключать риск грудного вскармливания, поэтому во время лечения кабозантинибом и по крайней мере в течение 4 месяцев после завершения лечения необходимо прекратить грудное вскармливание.
Фертильность
Данных о влиянии кабозантиниба на фертильность человека нет. Результаты исследований указывают на то, что кабозантиниб может негативно повлиять на фертильность у мужчин и женщин. Мужчинам и женщинам необходимо использовать эффективные методы контрацепции при лечении.
Безопасность и эффективность кабозантиниба для детей и подростков (<18 лет) не установлены. Соответствующие данные отсутствуют. Не использовать детям.
Почечноклеточная карцинома (НКК)
КАБОМЕТИКС показан для лечения распространенной почечноклеточной карциномы (НКК):
- у взрослых пациентов, ранее не получавших лечение и имеющих средний или высокий риск (см. раздел «Фармакодинамические свойства»);
- у взрослых пациентов после предварительного лечения средствами, влияющими на фактор роста эндотелия сосудов (VEGF).
Гепатоцеллюлярная карцинома (ГЦК)
КАБОМЕТИКС показан как монотерапия гепатоцеллюлярной карциномы (ГЦК) у взрослых пациентов, ранее получавших лечение сорафенибом.
Гиперчувствительность к действующему веществу или любому из вспомогательных веществ лекарственного средства.
Лечение лекарственным средством КАБОМЕТИКС должен назначать и проводить врач, имеющий опыт назначения противоопухолевых лекарственных средств.
Способ применения
Кабометикс предназначен для перорального применения. Таблетки глотают целиком, не измельчая. Пациентам не следует употреблять пищу за 2 ч до и по крайней мере 1 ч после приема лекарственного средства КАБОМЕТИКС.
Дозы
Рекомендуемая доза Кабометикса для лечения НКК и ГЦК составляет 60 мг один раз в сутки.
Лечение лекарственным средством следует продолжать до момента прекращения получения пациентом клинических преимуществ от терапии или до появления недопустимых признаков токсичности.
Возникновение подозреваемых побочных реакций на лекарственное средство может потребовать временного прекращения лечения и/или снижения дозы КАБОМЕТИКС (см. таблицу 5). В случае необходимости, дозу рекомендуется уменьшить до 40 мг/сут, а затем до 20 мг/сут.
При развитии токсичности 3 степени по классификации СТСАЭ (Единые терминологические критерии побочных реакций) или выше или при развитии непереносимой токсичности 2 степени необходимо временно приостановить лечение. При серьезных или непереносимых проявлениях токсичности рекомендуется снизить дозу.
Пропущенную дозу следует принимать, если до приема следующей дозы осталось менее 12 часов.
Таблица 5
Рекомендуемые модификации доз лекарственного средства КАБОМЕТИКС и необходимые меры при развитии побочных реакций
Побочная реакция и степень тяжести
Рекомендуемые изменения дозы и мероприятия
Побочные реакции 1–2 степени, хорошо переносимые и легко лечащиеся
Не нужно корректировать дозу.
Начать поддерживающую терапию по показаниям.
Побочные реакции 2 степени, непереносимые, не исчезающие после снижения дозы или назначения поддерживающей терапии
Прекратить лечение, пока токсичность не снизится до 1 степени.
Показано начать поддерживающую терапию по показаниям.
Рассмотреть возможность восстановления терапии в меньшей дозе.
Побочные реакции 3 степени (за исключением клинически неподходящих лабораторных отклонений)
Прекратить лечение, пока токсичность не снизится до 1 степени.
Показано начать поддерживающую терапию по показаниям.
Восстановить терапию в меньшей дозе.
Побочные реакции 4 степени (за исключением клинически неподходящих лабораторных отклонений)
Приостановить лечение.
Оказать соответствующую медицинскую помощь.
При уменьшении токсичности до 1 степени, восстановить терапию в меньшей дозе.
Если побочные реакции сохраняются, окончательно отменить лечение лекарственным средством КАБОМЕТИКС.
Примечание: Критерии оценки степени тяжести побочных реакций согласно NCI-CTCAE v4.
Сопутствующие лекарственные средства
Следует с осторожностью сопутствовать лекарственным средствам, являющимся сильными ингибиторами СYP3A4, и следует избегать постоянного сопутствующего применения лекарственных средств, являющихся сильными индукторами CYP3A4 (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Следует учитывать выбор альтернативного сопутствующего лекарственного средства, не имеющего или имеющего минимальную ингибирующую активность по влиянию на изофермент CYP3A4.
Особые группы пациентов
Пациенты пожилого возраста
Не требуется корректировка дозы кабозантиниба у пациентов пожилого возраста (≥ 65 лет).
Этническая принадлежность
Этническая принадлежность не требует корректировки дозы (см. раздел Фармакокинетика).
Пациенты с почечной недостаточностью
Кабозантиниб следует назначать с осторожностью пациентам с почечной недостаточностью легкой или умеренной степени.
Кабозантиниб противопоказан пациентам с почечной недостаточностью тяжелой степени, поскольку безопасность и эффективность кабозантиниба для этой популяции больных не установлены.
Пациенты с печеночной недостаточностью
Пациентам с печеночной недостаточностью легкой степени корректировки дозы не требуется. Поскольку имеются только ограниченные данные о применении кабозантиниба у пациентов с печеночной недостаточностью умеренной степени (В по шкале Чайлда – Пью), невозможно дать рекомендации по дозировке. Для этих пациентов рекомендуется обеспечить мониторинг общей безопасности (см. раздел «Фармакокинетика»). Учитывая отсутствие клинического опыта применения кабозантиниба у пациентов с печеночной недостаточностью тяжелой степени (С по шкале Чайлда – Пью), кабозантиниб не рекомендуется применять в этой категории пациентов (см. раздел «Фармакокинетика»).
Пациенты с сердечной недостаточностью
Данные по применению пациентам с сердечной недостаточностью ограничены. Не существует конкретных рекомендаций по дозировке для этой популяции пациентов.
Краткое описание профиля безопасности
Наиболее распространенными серьезными побочными реакциями у пациентов с НКК (частота ≥ 1%) являются диарея, артериальная гипертензия, обезвоживание, гипонатриемия, тошнота, снижение аппетита, эмболия, утомляемость, гипомагниемия, синдром ладонно-подошовенной эритродизестезии.
Наиболее распространенными побочными реакциями любой степени (наблюдавшими по меньшей мере у 25% пациентов) среди больных НКК были диарея, артериальная гипертензия, утомляемость, повышение АСТ, повышение АЛТ, тошнота, снижение аппетита, СДПЭ, дисгевзия, снижение уровня тромбоцитов. анемия, рвота, снижение массы тела, диспепсия и закреп. Артериальную гипертензию наблюдали чаще у пациентов с НКК, ранее не получавших лечение (67%), по сравнению с больными НКК, которым ранее применяли средства, влияющие на VEGF (37%).
Наиболее распространенными серьезными побочными реакциями у пациентов с ГЦК (частота ≥ 1%) являются печеночная энцефалопатия, синдром ладонно-подошвенной эритродизестезии, астения и диарея. Наиболее распространенными побочными реакциями любой степени (наблюдавшими по меньшей мере у 25% пациентов) среди больных ГЦК были диарея, синдром ладонно-подошвенной эритродизестезии, утомляемость, снижение аппетита, артериальная гипертензия и тошнота. Список побочных реакций приведен в таблице 6.
В таблице 6 побочные реакции распределены по классам систем органов согласно терминологии MedDRA и классифицированы по частоте по данным обо всех степенях тяжести следующим образом: очень часто (≥ 1/10), часто (≥ 1/100 и < 1/10), нечасто (≥ 1/1000 и < 1/100), неизвестно (невозможно определить по имеющимся данным). В пределах каждой группы по частоте побочные реакции представлены в порядке уменьшения их серьезности.
Таблица 6
Побочные реакции на лекарственное средство (ПРЛС), зарегистрированные при применении кабозантиниба в клинических исследованиях
Система органов (по MedDRA)
Очень часто
Часто
Нечасто
Неизвестно
Инфекции и инвазии
абсцесс
Со стороны кровеносной и лимфатической систем
анемия
нейтропения тромбоцитопения
лимфопения
Со стороны органов эндокринной системы
гипотиреоз
Со стороны метаболизма и пищеварительной системы
снижение аппетита
гипомагниемия
гипокалиемия
дегидратация
гипоальбуминемия
гипофосфатемия
гипонатриемия
гипокальциемия гиперкалиемия гипербилирубинемия
гипергликемия
гипогликемия
Со стороны нервной системы
дисгевзия
головная боль
головокружение
периферическая сенсорная нейропатия
судороги
церебровас-кулярное нарушение
Со стороны органов слуха и равновесия
тинитус
Со стороны сердца
инфаркт миокарда
Со стороны сосудистой системы
артериальная гипертензия
кровоизлияния
венозный тромбоз
артериальный тромбоз
Со стороны дыхательной системы, органов грудной клетки и средостения.
дисфония
одышка кашель
легочная эмболия
Со стороны пищеварительной системы
диарея
тошнота
рвота
стоматит
запор
боли в животе диспепсия боли в верхних отделах живота
перфорация желудочно-кишечного тракта фистула
гастроэзофагальный рефлюкс
геморрой
боль в полости рта
сухость во рту
панкреатит глосалгия
Со стороны гепатобилиарной системы
печеночная энцефалопатия
холестатический гепатит
Со стороны кожи и подкожной клетчатки
синдром ладонно-подошвенной эритродизес-тезии
сыпь
зуд
алопеция
сухость кожи акнеформный дерматит
изменение цвета волос
Со стороны скелетно-мышечной системы и соединительной ткани
боль в конечностях
мышечные спазмы
артралгия
остеонекроз челюсти
Со стороны почек и мочевыводящих путей
протеинурия
Общие нарушения
утомляемость воспаления слизистых оболочек астения периферический отек
Со стороны лабораторных показателей
снижение массы тела
повышение уровня аланинамино-трансферазы (АЛT) в сыворотке крови
повышение уровня аспартатамино-трансферазы (АСT) в сыворотке крови
повышение уровня щелочной фосфатазы (ЛФ) в крови повышение уровня гамма-глутамилтрансферазы (ГГТ)
повышение уровня креатинина в крови
повышение уровня амилазы повышение уровня липазы
повышение уровня холестерина в крови
снижение уровней лейкоцитов
повышение уровней триглицеридов в крови
Травмы, отравления и осложнения, вызванные при проведении процедур
осложнение заживления ран
Описание отдельных побочных реакций
Данные относительно нижеперечисленных реакций у пациентов, принимавших лекарственное средство КАБОМЕТИКС в дозе 60 мг/сут (перорально), получены во время базисных исследований с участием пациентов с НКК после терапии на основе лекарственных средств, влияющих на VEGF, и НКК, ранее не получали лечение, а также с участием пациентов с ГЦК после предварительной системной терапии (см. раздел Фармакодинамика).
Перфорация желудочно-кишечного тракта
В исследовании НКК после применения лекарственных средств, влияющих на VEGF (METEOR), перфорация ЖКТ степени 2 или 3 была зарегистрирована у 0,9% пациентов с почечноклеточной карциномой, получавших лечение кабозантинибом (у 3 из 331). Медиана времени до появления перфораций составляла 10 недель.
В исследовании НКК с участием пациентов, ранее не получавших лечение (CABOSUN), перфорацию ЖКТ степени 4 и 5 выявили у 2,6% (у 2 из 78) пациентов, получавших кабозантиниб.
В исследовании ГЦК (CELESTIAL) перфорацию ЖКТ степени 3 или 4 обнаружили у 0,9% пациентов, которых лечили кабозантинибом (4 из 467). Медиана времени до появления перфораций составляла 5,9 недели.
В клинической программе исследования кабозантиниба отмечались случаи перфорации с летальным исходом.
Печеночная энцефалопатия
В исследовании ГЦК (CELESTIAL) печеночную энцефалопатию (печеночную энцефалопатию, энцефалопатию, гипераммонимическую энцефалопатию) отмечали у 5,6% пациентов, получавших кабозантиниб (26 из 467). Реакции степени 3-4 наблюдали у 2,8%; также зафиксирован один случай ступени 5 (0,2%). Медиана времени до развития энцефалопатии составляла 5,9 недели. В исследованиях НКК (METEOR и CABOSUN) случаев печеночной энцефалопатии не зафиксировано.
Диарея
В исследовании НКК после предварительной терапии средствами, влияющими на VEGF (METEOR), диарею обнаружено у 74% пациентов, получавших кабозантиниб (245 из 331). Реакции степени 3 – 4 составили 11%. Медиана времени до появления диареи составляла 4,9 недели.
В исследовании НКК среди пациентов, ранее не получавших лечение (CABOSUN), диарею наблюдали у 73% пациентов, получавших кабозантиниб (57 из 78). Реакции степени 3 – 4 зафиксированы в 10% случаев.
В исследовании ГЦК (CELESTIAL) диарею наблюдали у 54% пациентов, получавших кабозантиниб (251 из 467); реакции степени 3-4 зафиксированы в 9,9%. Медиана времени до появления всех этих случаев составила 4,1 недели. В результате диареи у 84 из 467 (18%), 69 из 467 (15%) и у 5 из 467 (1%) пациентов пришлось изменять дозу, прекратить терапию и полностью отменить лечение соответственно.
Фистулы
В исследовании НКК после предварительной терапии средствами, влияющими на VEGF (METEOR), фистулы наблюдались у 1,2% (у 4 из 331) пациентов, принимавших кабозантиниб, в частности фистулы прямой кишки у 0,6% (у 2 из 331). Один случай классифицирован как побочная реакция 3 степени, а остальной – как реакции 2 степени. Медиана времени до появления фистулы составила 30,3 недели.
В исследовании НКК с участием пациентов, ранее не получавших лечение (CABOSUN), фистулы не обнаружили.
В исследовании ГЦК (CELESTIAL) фистулы наблюдали у 1,5% (7 из 467) больных ГЦК. Медиана времени до появления фистулы составляла 14 недель.
В программе клинической разработки кабозантиниба сообщали о случаях фистул с летальным исходом.
Кровотечение
В исследовании НКК после предварительной терапии средствами, влияющими на VEGF (METEOR), частота возникновения тяжелых геморрагических событий (степень ≥ 3) составила 2,1% у пациентов с НКК, получавших кабозантиниб (7 из 331). Медиана времени до начала кровотечения составила 20,9 недель.
В исследовании НКК с участием пациентов, ранее не получавших лечение (CABOSUN), частота возникновения тяжелых геморрагических событий (степень ≥ 3) составила 5,1% (4/78) среди пациентов с НКК, получавших кабозантиниб.
В исследовании ГЦК (CELESTIAL) частота возникновения тяжелых геморрагических событий (степень ≥ 3) составила 7,3% у пациентов, получавших кабозантиниб (34 из 467). Медиана времени до начала кровотечения составляла 9,1 нед.
В программе клинической разработки кабозантиниба сообщали о случаях кровотечения со смертельным исходом.
Синдром обратимой задней лейкоэнцефалопатии (СОЗЛ)
В исследованиях METEOR, CABOSUN или CELESTIAL не было сообщений о случаях СОЗЛ, но в других клинических исследованиях изредка сообщалось о случаях СОЗЛ (у 2 из 4872 пациентов; 0,04%).
Сообщение о побочных реакциях
▼Это лекарственное средство является объектом дополнительного мониторинга.
Сообщения о побочных реакциях после регистрации лекарственного средства важны. Это обеспечивает постоянный мониторинг соотношения польза/риск лекарственного средства. Медицинских работников просят сообщать о любых подозреваемых побочных реакциях через национальную систему сообщений.
Специального лечения при передозировке кабозантинибом не существует, а возможные симптомы передозировки не установлены. При подозрении на передозировку прием кабозантиниба следует прекратить и начать поддерживающую терапию. Необходим контроль лабораторных биохимических показателей и параметров метаболизма и мониторинг их по крайней мере еженедельно или при наличии клинических показаний. Побочные реакции, связанные с передозировкой, лечат симптоматически.
- Лекарственное средство не нуждается в особых условиях хранения. Хранить в недоступном для детей месте.
Препарат Кабометикс® предназначен для лечения распространённого почечно-клеточного рака: у взрослых пациентов с промежуточным или плохим прогнозом, не получавших ранее терапию; у взрослых пациентов после предшествующей терапии антиангиогенными препаратами (VEGF-таргетная терапия).
Часто задаваемые вопросы
- Действующие вещества в Кабометикс 60 мг №30 таблетки является Кабозантиниб
- Кабометикс 60 мг №30 таблетки с осторожностью принимать перед управлением транспорта
- Кабометикс 60 мг №30 таблетки запрещено принимать беременным
- Кабометикс 60 мг №30 таблетки запрещено принимать во время грудного вскармливания
- Кабометикс 60 мг №30 таблетки принимать аллергетикам
- Кабометикс 60 мг №30 таблетки принимать диабетикам
- Рекомендуемая температура хранения Кабометикс 60 мг №30 таблетки
- Рекомендуемый срок хранения Кабометикс 60 мг №30 таблетки 3 года
Отзывы о товаре
Еще нет отзывов о товаре. Будь первым, кто оставит отзыв.